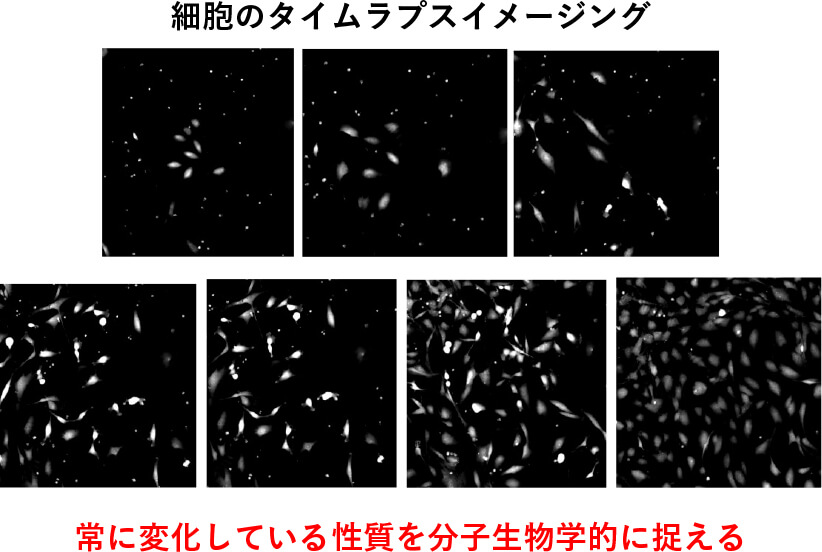
神経再生研究チーム
Neural Regeneration Research Team| チームリーダー | 篠崎 宗久(特任准教授) |
|---|---|
| 研究ターゲット | 脳・脊髄の損傷・障害 |
| 研究目的 | iPSC由来神経幹細胞・遺伝子治療を用いた、脳・脊髄の機能再生 |
| 主な研究トピック |
・霊長類,げっ歯類における脊髄損傷モデル動物の病態解明 |
主な研究成果
【研究室の道のり】
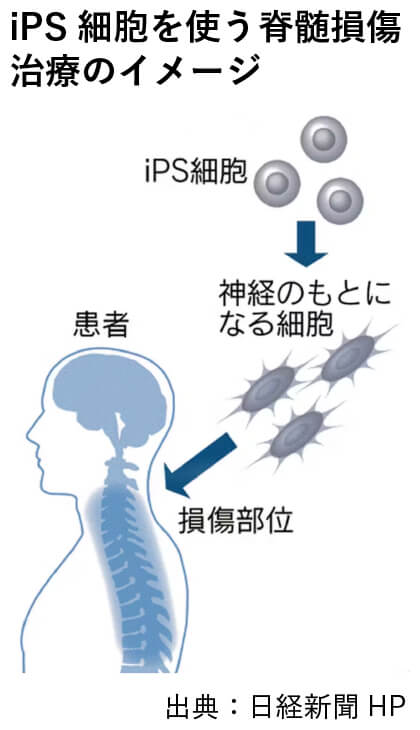
私たちは、これまで20年間、整形外科学教室の中村雅也教授たちと協力しながら、脊髄損傷の治療方法を研究してきました。研究では、神経組織の元となる神経幹細胞を、傷ついた脊髄に移植すると機能が回復することを早い段階で見出していました。しかし当時、日本では倫理上の問題で神経幹細胞の元の細胞として用いていたESC(Embryonic Stem cell)を用いることは出来ませんでした。そこで2006年、まだノーベル賞受賞前の山中伸弥先生との共同研究を開始し、以降、iPSC(induced Pluripotent Stem cell)由来神経幹細胞を用いた研究を続けております。
【臨床試験の開始】
【真の再生のために】
神経難病研究チーム
Intractable Neurological Disease Research Team| チームリーダー | 森本 悟(特任准教授/副センター長) |
|---|---|
| 研究ターゲット | 筋萎縮性側索硬化症(Amyotrophic Lateral Sclerosis (ALS))およびその他の神経難病 |
| 研究目的 | 疾患特異的iPS細胞およびヒト生体・剖検試料を用いた、ヒト神経系病態の解明と創薬を目的とする |
| 主な研究トピック |
・ヒト疾患モデルを用いたiPS細胞創薬と遺伝子治療 |
主な研究成果
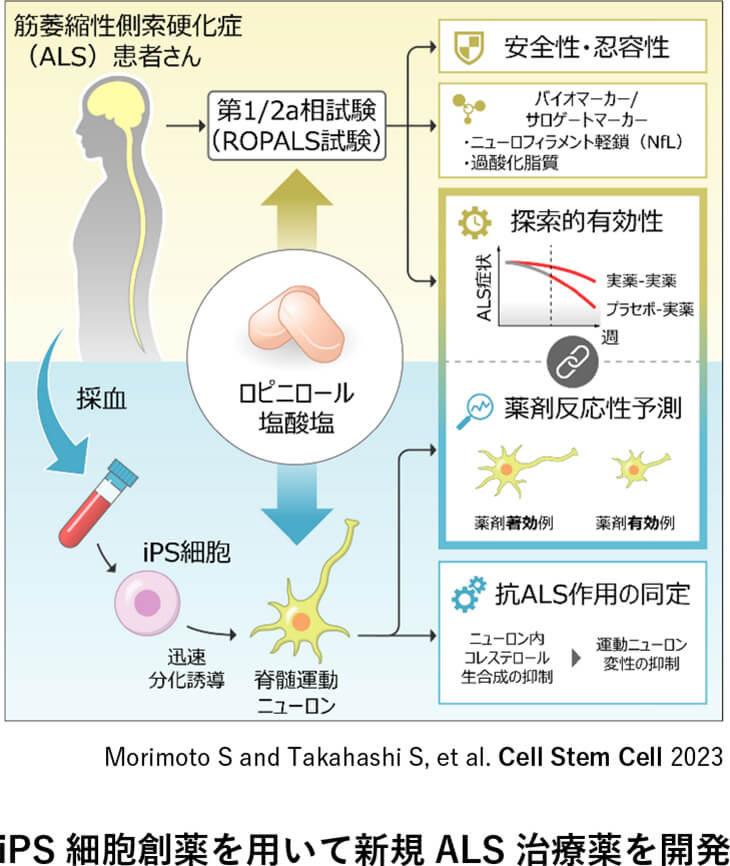
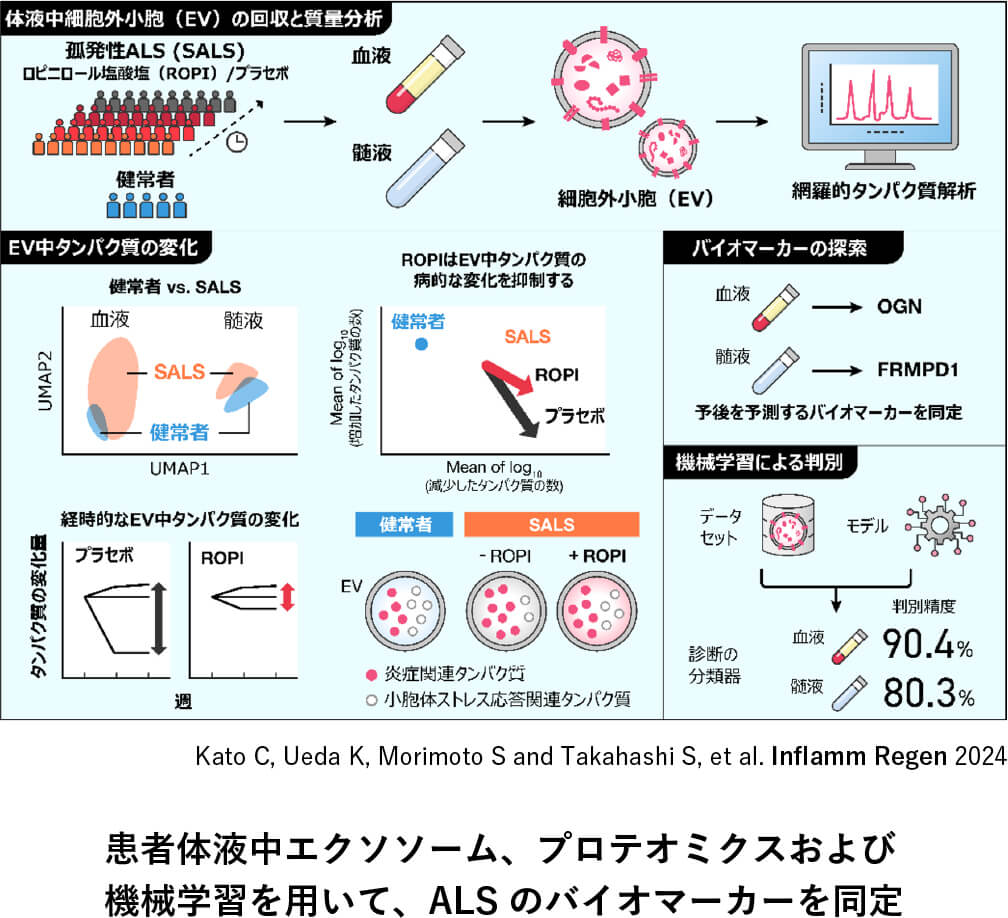
主な業績
・Qi C, Verheijen BM, Kokubo Y, Shi Y, Tetter S, Murzin AG, Nakahara A, Morimoto S, Vermulst M, Sasaki R, Aronica E, Hirokawa Y, Oyanagi K, Kakita A, Ryskeldi-Falcon B, Yoshida M, Hasegawa M, Scheres SHW, Goedert M. Tau Filaments from Amyotrophic Lateral Sclerosis/Parkinsonism-Dementia Complex (ALS/PDC) adopt the CTE Fold. Proc Natl Acad Sci U S A 2023 ;120(51):e2306767120.
・Okano H, Morimoto S, Kato C, Nakahara J, Takahashi S. Induced pluripotent stem cells-based disease modeling, drug screening, clinical trials, and reverse translational research for amyotrophic lateral sclerosis. J Neurochem. 2023 Dec;167(5):603-614.
・Li D, Johmura Y, Morimoto S, Doi M, Nakanishi K, Ozawa M, Tsunekawa Y, Inoue-Yamauchi A, Naruse H, Matsukawa T, Takeshita Y, Suzuki N, Aoki M, Nishiyama A, Zeng X, Konishi C, Suzuki N, Nishiyama A, Harris AS, Morita M, Yamaguchi K, Furukawa Y, Nakai K, Tsuji S, Yamazaki S, Yamanashi Y, Shimada S, Okada T, Okano H, Toda T, Nakanishi M. LONRF2 is a protein quality control ubiquitin ligase whose deficiency causes late-onset neurological deficits. Nat Aging 2023 Aug;3(8):1001-1019.
・Morimoto S*, Takahashi S*, Ito D, Daté Y, Okada K, Kato C, Nakamura S, Ozawa F, Chai MC, Nishiyama A, Suzuki N, Fujimori K, Kondo T, Takao M, Hirai M, Kabe Y, Suematsu M, Jinzaki M, Aoki M, Fujiki Y, Sato Y, Suzuki N, Nakahara J, Okano H. Phase 1/2a clinical trial in ALS with ropinirole, a drug candidate identified by iPSC drug discovery. Cell Stem Cell 2023 Jun 1;30(6):766-780.e9. (*equally contributed)
・Morimoto S*, Saeki K*, Takeshita M, Hirano K, Shirakawa M, Yamada Y, Nakamura S, Ozawa F, Okano H. Intranasal Sendai virus-based SARS-CoV-2 vaccine using a mouse model. Genes Cells 2023 Jan;28(1):29-41. (*equally contributed)
・Ito D, Morimoto S, Takahashi S, Okada K, Nakahara J, Okano H. Maiden voyage: induced pluripotent stem cell-based drug screening for amyotrophic lateral sclerosis. Brain. 2023 Jan 5;146(1):13-19.
・Okano H and Morimoto S. iPSC-based disease modeling and drug discovery in cardinal neurodegenerative disorders. Cell Stem Cell 2022;29(2):189-208.
・Morimoto S, Takahashi S, Fukushima K, Saya H, Suzuki N, Aoki M, Okano H, Nakahara J. Ropinirole hydrochloride remedy for amyotrophic lateral sclerosis - Protocol for a randomized, double-blind, placebo-controlled, single-center, and open-label continuation phase I/IIa clinical trial (ROPALS trial). Regen Ther 2019;11:143-166.
・Ishiura H, Shibata S, Yoshimura J, Suzuki Y, Qu W, Doi K, Almansour MA, Kikuchi JK, Taira M, Mitsui J, Takahashi Y, Ichikawa Y, Mano T, Iwata A, Harigaya Y, Matsukawa MK, Matsukawa T, Tanaka M, Shirota Y, Ohtomo R, Kowa H, Date H, Mitsue A, Hatsuta H, Morimoto S, Murayama S, Shiio Y, Saito Y, Mitsutake A, Kawai M, Sasaki T, Sugiyama Y, Hamada M, Ohtomo G, Terao Y, Nakazato Y, Takeda A, Sakiyama Y, Umeda-Kameyama Y, Shinmi J, Ogata K, Kohno Y, Lim SY, Tan AH, Shimizu J, Goto J, Nishino I, Toda T, Morishita S, Tsuji S. Noncoding CGG repeat expansions in neuronal intranuclear inclusion disease, oculopharyngodistal myopathy and an overlapping disease. Nat Genet 2019;51:1222-1232.
組織再生研究チーム
Tissue Regeneration Research Team| チームリーダー | 八代 嘉美(慶應義塾大学 特任教授/藤田医科大学 教授) |
|---|---|
| 研究ターゲット | 組織再生に関わる細胞集団の特性解析と分裂行動パターンニング |
| 研究目的 | iPS細胞およびヒト生体試料を用いた、ヒト組織幹細胞の品質評価に関わるエビデンス構築 |
| 主な研究トピック |
・iPS細胞およびヒト生体試料からの組織幹細胞の分離・誘導
|
主な研究成果
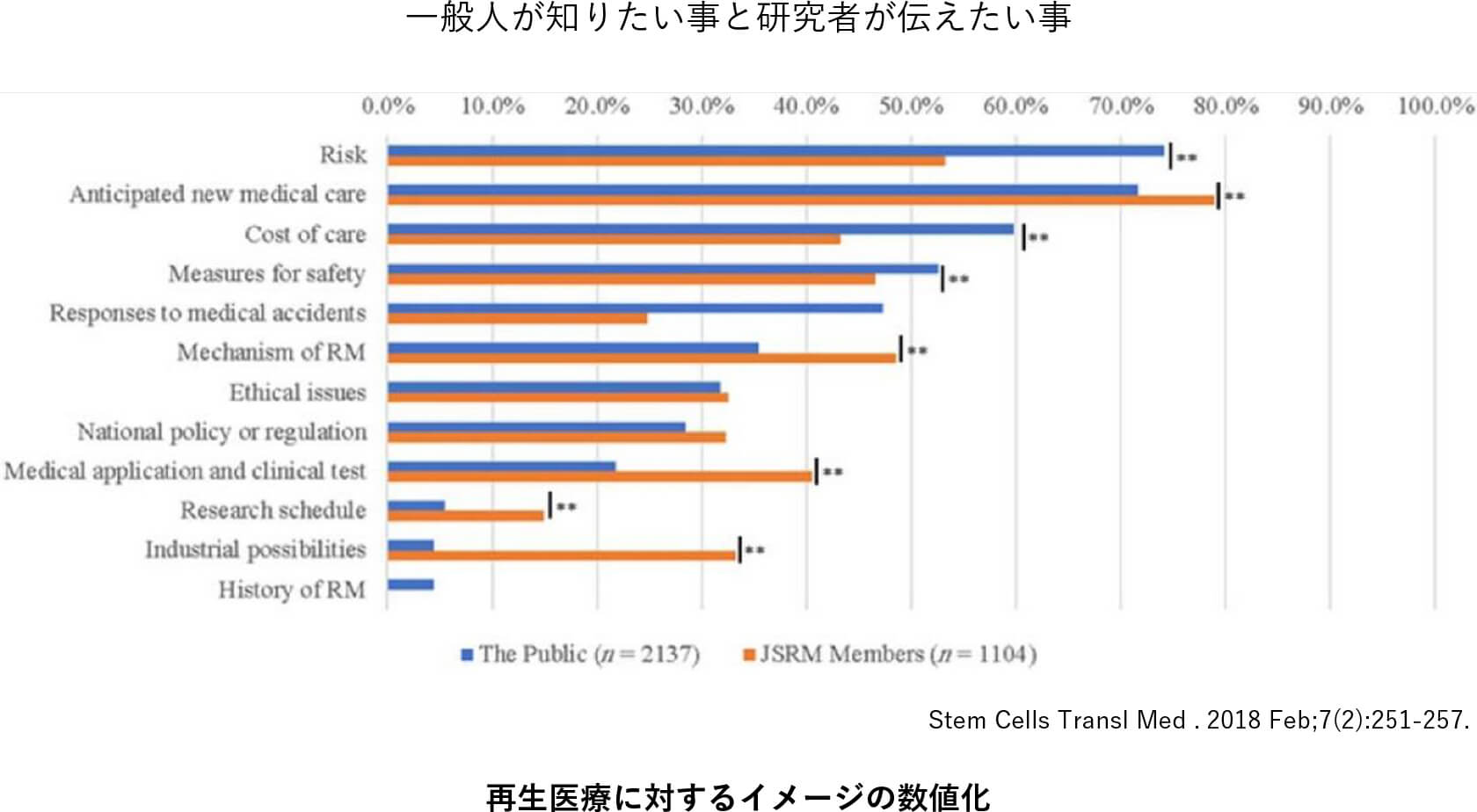

主な業績
・Ludwig TE, Kujak A, Rauti A, Andrzejewski S, Langbehn S, Mayfield J, Fuller J, Yashiro Y, Hara Y, Bhattacharyya A. 20 Years of Human Pluripotent Stem Cell Research: It All Started with Five Lines. Cell Stem Cell. 2018 Nov 1;23(5):644-648.
・Inoue Y, Shineha R, Yashiro Y. Current Public Support for Human-Animal Chimera Research in Japan Is Limited, Despite High Levels of Scientific Approval. Cell Stem Cell. 2016 Aug 4;19(2):152-153
・Ikka T, Fujita M, Yashiro Y, Ikegaya H. Recent Court Ruling in Japan Exemplifies Another Layer of Regulation for Regenerative Therapy. Cell Stem Cell. 2015 Nov 5;17(5):507-8.
ヒト脳器官発生チーム
Human Brain Organogenesis TeamーCortical development and neuropsychiatric disordersー
| チームリーダー | 嶋田 弘子 (慶應義塾大学 殿町先端研究教育連携スクエア 特任講師) (大阪大学 ヒューマン・メタバース疾患研究拠点 招へい准教授) |
|---|---|
| 研究目的 | ヒトiPS細胞由来の大脳皮質オルガノイドを用いた、中枢神経発生メカニズムの解明、 および、精神神経疾患モデル作製と病態メカニズムの解明、創薬への応用 |
| 主な研究トピック |
1.認知症モデル大脳皮質オルガノイドの作製と病態メカニズムの解明、創薬研究への応用 |
主な研究成果
【タウ凝集モデル、アルツハイマー病(AD)モデル脳オルガノイドの作製】
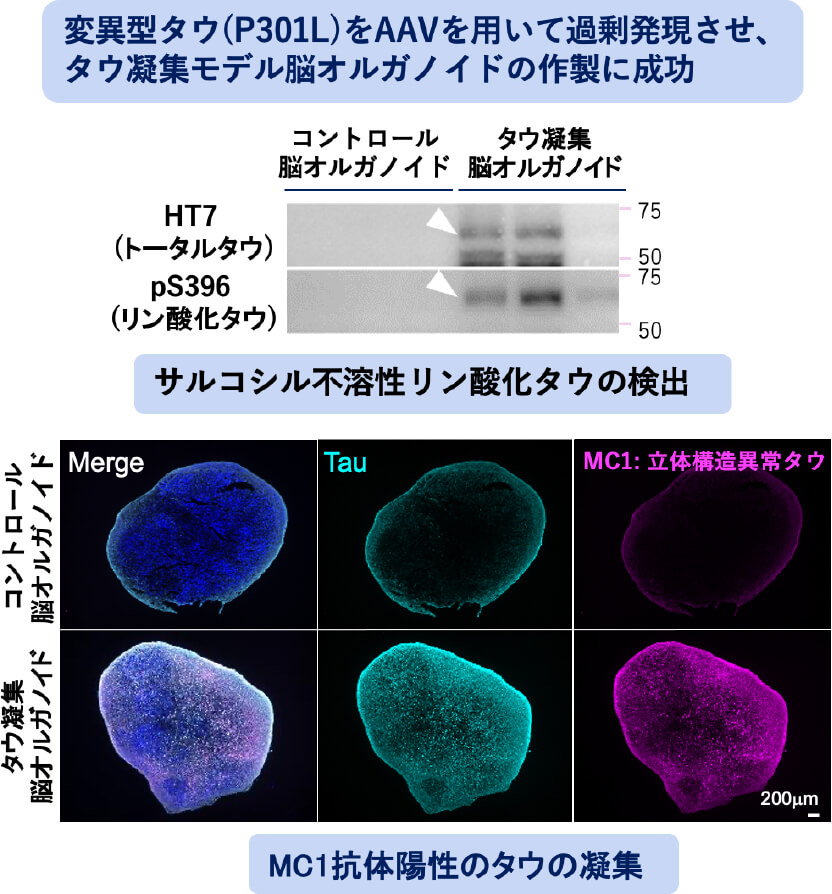
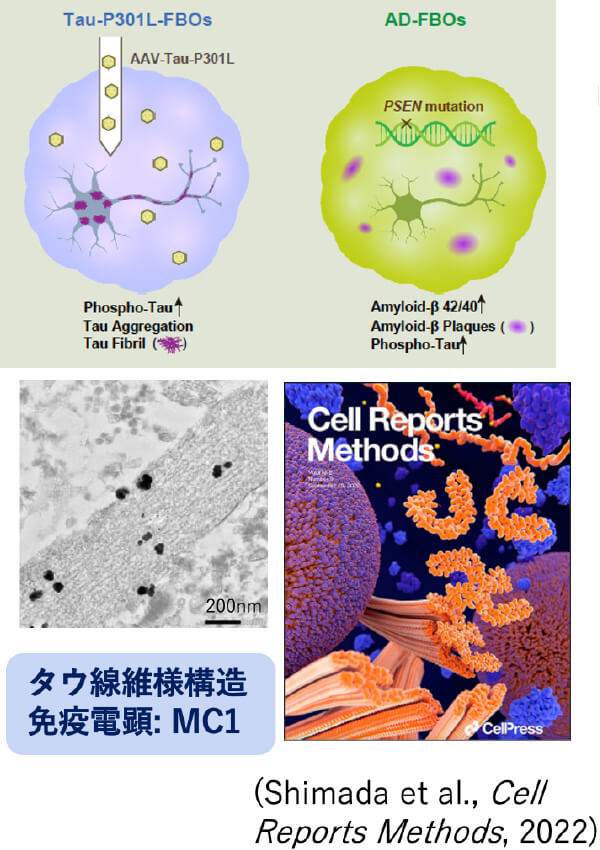
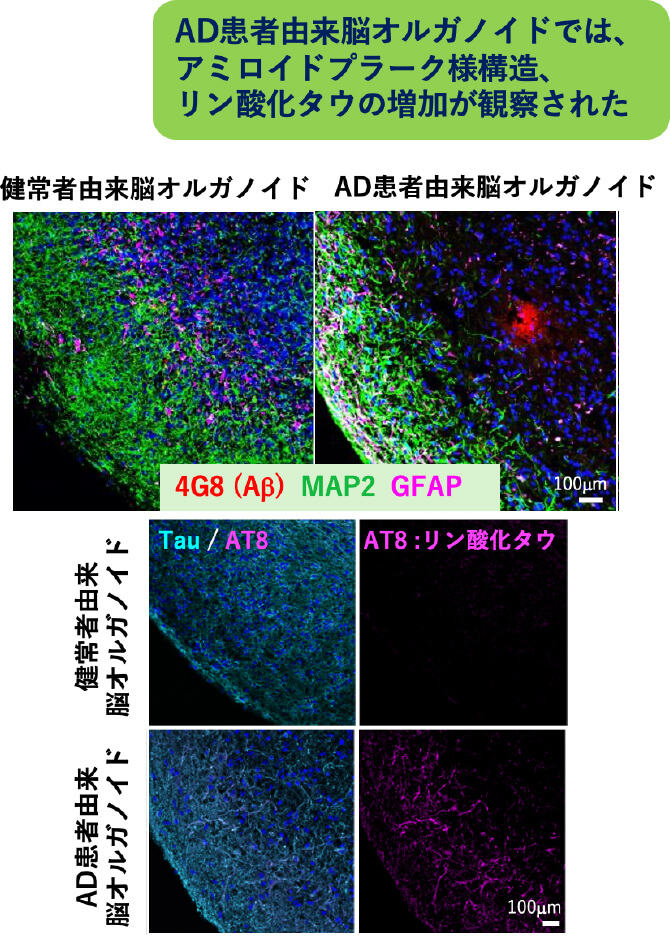
主な業績
・Holly Y. Chen, Manju Swaroop, Samantha Papal, Anupam K. Mondal, GregoryJ. Tawa, Florian Regent, Hiroko Shimada, Kunio Nagashima, Natalia de Val, Samuel G. Jacobson, Wei Zheng, Anand Swaroop. Reserpine maintains photoreceptor survival in retinal ciliopathy by resolving proteostasis imbalance and ciliogenesis defects. eLife, 12: e83205 (2023)
・Hirosato Ideno, Kent Imaizumi, Hiroko Shimada, Tsukasa Sanosaka, Akisa Nemoto, Jun Kohyama, Hideyuki Okano. Human PSCs determine the competency of cerebral organoid differentiation via FGF signaling and epigenetic mechanisms. iScience, 25(10):105140 (2022)
・Hiroko Shimada, Yuta Sato, Takashi Sasaki, Aki Shimozawa, Kent Imaizumi, Tomoko Shindo Takahiro Kondo, Shinsuke Shibata, Junro Kuromitsu, Hirofumi Aoyagi, Daisuke Ito and Hideyuki Okano. A next-generation iPSC-derived forebrain organoid model of tauopathy with tau fibrils by AAV-mediated gene transfer. Cell Reports Methods, 2, 100289 (2022)
・Kamil Kruczek*, Zepeng Qu*, Emily Welby*, Hiroko Shimada, Suja Hiriyanna, Milton A. English, Wadih M. Zein, Brian P. Brooks and Anand Swaroop. In vitro modeling and rescue of ciliopathy associated with mutations in IQCB1 (Nephrocystin 5) using patient-derived cells. Stem Cell Reports, 17, 10 (2022), * These authors equally contributed.
・Hiroko Shimada, Quanlong Lu, Christine Insinna-Kettenhofen, Kunio Nagashima, Milton A. English, Elizabeth M. Semler, Jacklyn Mahgerefteh, Artur V. Cideciyan, Tiansen Li, Brian P. Brooks, Meral Gunay-Aygun, Samuel G. Jacobson, Tiziana Cogliati, Christopher J. Westlake, and Anand Swaroop. In vitro modeling using ciliopathy-patient-derived cells reveals distinct cilia dysfunctions caused by CEP290 mutations. Cell Reports, Vol. 20, p384-396 (2017)
マーモセット神経疾患モデル研究チーム
Marmoset Models of Brain Diseases Team| チームリーダー | 岸 憲幸(特任講師) |
|---|---|
| 研究ターゲット | レット症候群(Rett syndrome)およびその他の神経発達障害 |
| 研究目的 | 霊長類モデルマーモセットやiPS細胞を用いて、レット症候群や関連疾患の病態メカニズムの解明、治療法開発の土台作りを目的とする |
| 主な研究トピック |
・ゲノム編集技術を用いたレット症候群の霊長類モデルMECP2変異マーモセットの作製 |
主な研究成果
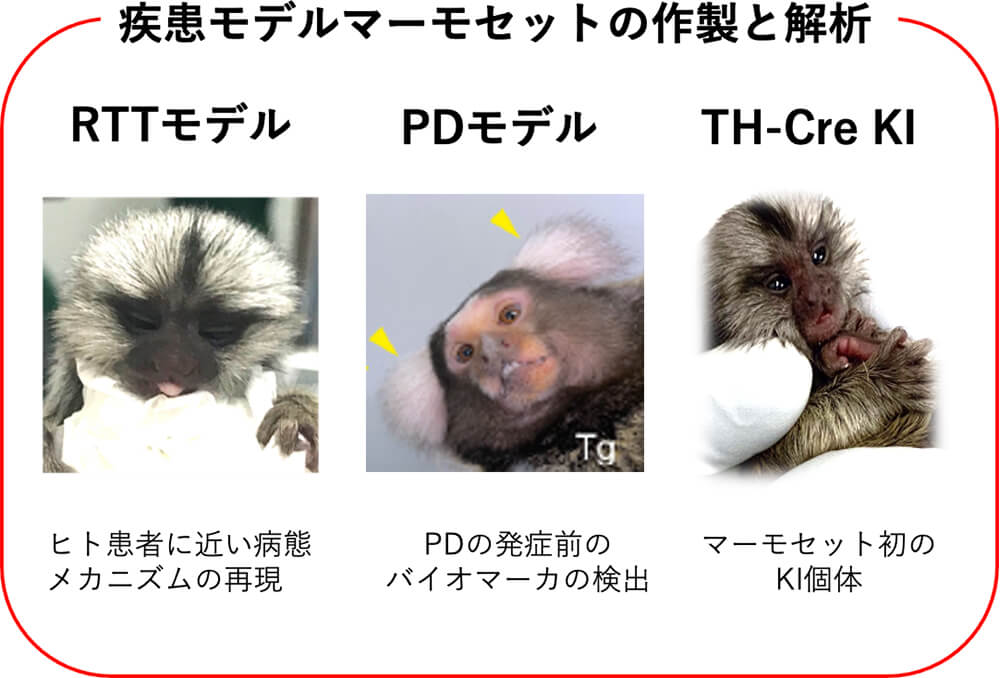
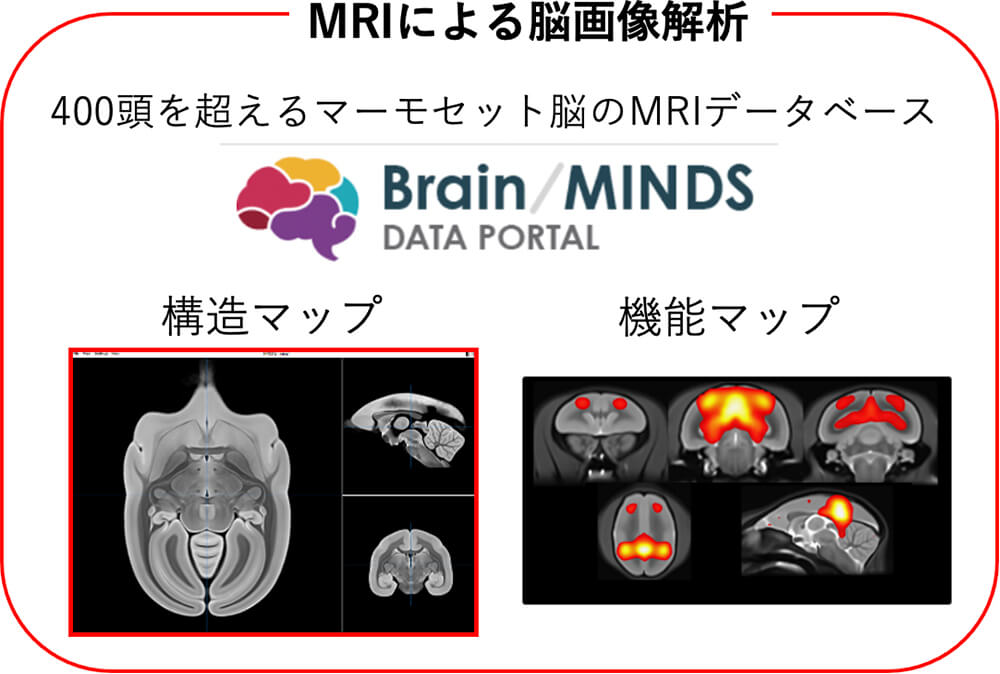
主な業績
・Okano H, Kishi N, Investigation of Brain Science and Neurological/Psychiatric Disorders Using Genetically Modified Non-Human Primates. Curr Opin Neurobiol, 2018
・Yoshimatsu S, et al., Generation of a Tyrosine hydroxylase (TH)-2A-Cre knock-in non-human primate model by homology-directed repair biased CRISPR-Cas9 genome editing. Cell Rep Methods, 2023.
・Hata J, et al., Multi-modal brain magnetic resonance imaging database covering marmosets with a wide age range. Scientific Data, 2023.